ARTIGOS ORIGINAIS
PROPORÇĂO DE LINFONODOS METASTÁTICOS COMO VARIÁVEL INDEPENDENTE DE PROGNÓSTICO NO CÂNCER COLORRETAL
Metastatic Lymph Node Ratio as an Independent Prognostic Variable in Colorectal Cancer
Denise Gonçalves Priolli1; Izilda Aparecida Cardinalli2; Camila Helaehil Alfredo3; Ana Paula Pimentel Spadari3; Felipe Rodrigues Máximo3; Nelson Fontana Margarido4; Carlos Augusto Real Martinez5
1Professor Adjunto Doutor do Curso de Medicina da Universidade São Francisco, Bragança Paulista, São Paulo, Brasil; 2 Professor Adjunto Doutor, Chefe da Disciplina de Patologia do Curso de Medicina da Universidade São Francisco, Bragança Paulista, São Paulo, Brasil; 3 Acadêmicos do Curso de Medicina da Universidade São Francisco, Bragança Paulista, São Paulo, Brasil; 4 Professor Livre-Docente do Departamento de Cirurgia da Universidade de São Paulo, São Paulo, Brasil; 5 Professor Adjunto Doutor do Curso de Pós-Graduação em Ciências da Saúde da Universidade São Francisco. Chefe do Serviço de Cirurgia Geral do Hospital Universitário São Francisco, Bragança Paulista, São Paulo, Brasil.
RESUMO: No câncer colorretal, o comprometimento linfonodal é um dos fatores prognósticos mais importantes. Objetivo: Determinar o valor prognóstico independentemente da relação entre linfonodos comprometidos e examinados em doentes com câncer colorretal. Método: Foram estudados 113 doentes (62 mulheres) portadores de câncer do cólon e reto superior. Quinze pertenciam ao estádio I da classificação TNM, 44 ao estádio II, 42 ao estádio III e 24 ao estádio IV. O índice de linfonodos comprometidos foi determinado pela relação entre número total de linfonodos comprometidos e examinados. Os doentes foram divididos segundo a proporção de linfonodos comprometidos em três grupos: ILC-0: sem comprometimento linfonodal; ILC-1: com comprometimento de até 20% dos linfonodos examinados; e ILC-2: com comprometimento neoplásico em 21% ou mais dos linfonodos examinados. As relações entre proporção de linfonodos comprometidos, número de linfonodos ressecados e número de linfonodos comprometidos foram determinadas. Excluíram-se doentes menores de 18 anos, submetidos à neoadjuvância e aqueles onde foram ressecados menos de 12 linfonodos. As variáveis anátomo-clínicas foram analisadas por estatística descritiva. A correlação entre as variáveis foi avaliada pelo teste de Spearman. A sobrevida foi determinada pelos testes de Kaplan-Meier, Log-rank e a análise multivariada pelo modelo de Cox estabelecendo nível de significância de 5%. Resultados: Houve diferença significante na sobrevida de cinco anos em doentes classificados nos diferentes grupos de ILC (p=0,009). Houve relação entre o número total de linfonodos comprometidos e o ILC (p=0,00001, com rs=0,977). Doentes do grupo ILC-0 apresentaram sobrevida global em cinco anos maior que 80%, enquanto os pertencentes aos grupos ILC-1 e ILC-2 a sobrevida global foi menor que 60% e 40%, respectivamente. O comprometimento linfonodal isolado apresentava-se relacionado à sobrevida em cinco anos (p=0,03). A análise multivariada demonstrou que o ILC é fator prognóstico independente (p=0,009). Conclusão: Os resultados do presente estudo permitem concluir que o ILC pode ser considerado uma variável independente preditora de sobrevida em doentes com câncer colorretal.
Descritores: Linfonodos, Excisăo de Linfonodo, Prognóstico, Neoplasias colorretais, Análise de sobrevida, Taxa de Sobrevida.
INTRODUÇÃO
O câncer colorretal (CCR) atualmente é o
segundo câncer mais prevalente em todo o mundo.
Estima-se que nos EUA sejam diagnosticados 153.760 casos novos por ano, e que em 2007 ocorreram
52.180 óbitos relacionados à
doença.(1) Nos últimos anos
variáveis clínicas, histopatológicas, moleculares e
genéticas têm sido relacionadas à sobrevida e a
sobrevida livre de doença em doentes com
CCR.(2-14) Assim, o diagnóstico
precoce,(2) a idade,(3) a localização
da neoplasia,(4) a graduação
histológica,(5) o grau de penetração na parede
intestinal,(6) o comprometimento
linfonodal,(7,8) a produção de muco pela
neoplasia,(9) os níveis pré-operatórios do
antígeno carcinoembrionário
(CEA),(10,11) a invasão
venosa,(12) neural,(13) e o perfil da expressão de vários
genes(14) são as variáveis mais estudadas, como fatores
relacionados ao prognóstico da doença. Apesar da
importância de todas essas variáveis, a invasão parietal, o
comprometimento linfonodal e a presença de
metástases, continuam representando a principal base de
predição da sobrevida e critério para instituição da
terapia adjuvante.(7) Embora estudos recentes venham
dando ênfase ao comprometimento linfonodal como
variável determinante relacionada ao prognóstico de
enfermos com CCR, questiona-se se a linfadenectomia
poderia realmente produzir efeito benéfico na sobrevida
dos doentes ou simplesmente seria procedimento que
traria apenas melhor acurácia no
estadiamento neoplasia.(15,16)
O efeito adverso do comprometimento dos linfonodos (LN) na sobrevida de doentes com
CCR tem sido uma das justificativas para a indicação de
terapia adjuvante em enfermos com doença
linfonodal. A menor sobrevida desses pacientes fez com que
a indicação de terapias adjuvantes fosse associada
ao tratamento cirúrgico, como forma de melhorar
estes índices, independentemente do número de LN
comprometidos. Dessa forma, doentes com apenas um
LN comprometido são submetidos ao mesmo protocolo
de tratamento adjuvante dos doentes com
envolvimento linfonodal mais extenso.
Estudos em portadores de CCR têm
reportado que tanto a sobrevida livre de doença quanto a
sobrevida global encontram-se relacionadas ao maior número
de LN ressecados.(17) Contudo, o número de LN
identificados no espécime cirúrgico encontra-se
diretamente relacionado à experiência do cirurgião durante
a ressecção da neoplasia, da técnica
histopatológica empregada para a sua recuperação, bem como da
experiência do patologista em
identificá-los.(18) Assim sendo, espécimes cirúrgicos com pequeno número
de LN ressecados ou identificados trazem insegurança
na determinação fidedigna do
comprometimento neoplásico e, conseqüentemente, na indicação do
tratamento adjuvante. Com o intuito de diminuir o
impacto da ressecção linfonodal tímida, vem sendo
estudada a importância da relação existente entre número
de LN ressecados e comprometidos pelo CCR. Estudos realizados em doentes com tumores primários do
estômago,(19,20)
bexiga,(21) mama,(22)
pâncreas(23) mostraram relação entre a proporção de LN
comprometidos, sobrevida livre de doença e a sobrevida global.
Da mesma forma, demonstrou-se que no carcinoma
gástrico, a proporção dos LN comprometidos em
relação aos examinados, índice de linfonodos
comprometidos (ILC), apresenta maior poder prognóstico quando
comparada a simples determinação do número de LN
comprometidos, adotada pelos diversos sistemas de
estadiamento.(24,25,26,27) Diante destas evidências,
o emprego do ILC vem sendo proposto com o objetivo de aprimorar e reduzir a margem preditiva de erro
em relação à sobrevida e intervalo livre de doença,
sobretudo em doentes onde o número de LN ressecados
ou examinados ficou aquém do limite mínimo
preconizado.(24, 25)
Poucos estudos avaliaram o ILC em relação
à sobrevida em doentes com CCR e, apenas em
dois deles, a avaliação do ILC foi independente do
estádio.(24,28) A validade do emprego do ILC como
variável relacionada a sobrevida do CCR ainda é
controversa. Alguns estudos não mostraram relação ente o ILC e
a sobrevida em portadores de CCR(28), enquanto
outros consideram o ILC mais importante do que a
simples presença do comprometimento
linfonodal.(20,23,24,29) Desta forma, a importância do ILC como fator
prognóstico independente do estadiamento no
câncer colorretal ainda merece ser melhor avaliada.
O objetivo do presente estudo foi examinar e determinar o impacto do ILC no prognóstico de
doentes com CCR.
MÉTODO
A realização do estudo obedeceu todas as
etapas previstas pelo Comitê de Ética em Pesquisa
da Universidade São Francisco e as exigências do
Conselho de Ética em Pesquisa da Comissão Nacional
de Ética em Pesquisa (CONEP) do Ministério da
Saúde (Resolução CNS196/96).
Trata-se de estudo retrospectivo, realizado por consulta à base de dados do Grupo de
Coloproctologia do Hospital Universitário São Francisco. Foram
considerados elegíveis para o estudo todos os enfermos
com diagnóstico de adenocarcinoma do cólon e reto alto
(localizados acima da reflexão peritonial),
classificados como pertencentes a quaisquer estádios da
classificação TNM onde foi realizada a ressecção completa
do tumor primário. Foram excluídos os menores de 18
anos e aqueles que apresentavam menos de 12 LN no
espécime cirúrgico
ressecado.(30) Também se excluíram
os portadores de tumor de reto médio e baixo por
terem sido submetidos a protocolo de
quimioradioterapia neoadjuvante. Após a seleção, de um total de 324
casos foram incluídos no estudo os registros de 113
doentes.
Da base de dados, foram anotadas as seguintes variáveis: idade (maior ou menor de 70 anos),
gênero (masculino ou feminino), raça (branca, negra
e amarela), grau histológico da neoplasia (bem,
moderadamente e pouco diferenciada), tipo da neoplasia
(produtor e não produtor de muco), invasão
angiolinfática (presente ou ausente), profundidade de invasão da
parede cólica (T1 a
T4) estadiamento patológico TNM
(I a IV), localização do tumor (cólon proximal, cólon
distal e reto alto), número de LN ressecados (média e
mediana), número de LN comprometidos
(N0, N1 e N2), tempo de seguimento após a cirurgia (em meses),
data do óbito, e sobrevida global.
As lâminas selecionadas, sempre coradas
pela técnica de hematoxilina-eosina (HE), foram
levantadas no Departamento de Patologia e revistas por
especialista experiente em neoplasias do trato digestivo
para confirmação do diagnóstico anatomopatológico e
revisão das variáveis histopatológicas consideradas. A
invasão da parede foi avaliada de acordo com a
profundidade do comprometimento mucoso, muscular,
da serosa ou do tecido adiposo adjacente. A
verificação de comprometimento neoplásico dos LN
ressecados foi avaliada pela técnica da HE não se utilizando
qualquer técnica imunoistoquímica para pesquisa
de micrometástases.
O cálculo do ILC foi determinado pela
razão entre número total de LN comprometidos e
examinados (ressecados), subdividindo-se os doentes em
três grupos segundo a porcentagem de
comprometimento linfonodal: ILC-0: 0%, quando não havia LN
comprometidos pela neoplasia; ILC-1: quando existia
comprometimento neoplásico em até 20% do número total
de LN ressecados; ILC-2: quando se encontrou mais
de 21% dos LN ressecados comprometidos pela
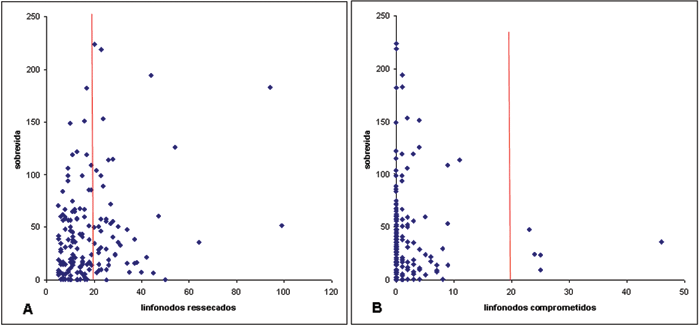
neoplasia. Tal estratificação foi obtida a partir de
cut-off de 20%, baseado no percentil 70, da população selecionada
para o estudo (Figura 1 A e B).
 |
Figura 1 - A - Distribuição da amostra elegível segundo o número de linfonodos ressecados. B - Distribuição da amostra elegível segundo o número de linfonodos comprometidos. Linha de corte em 20%. |
 |
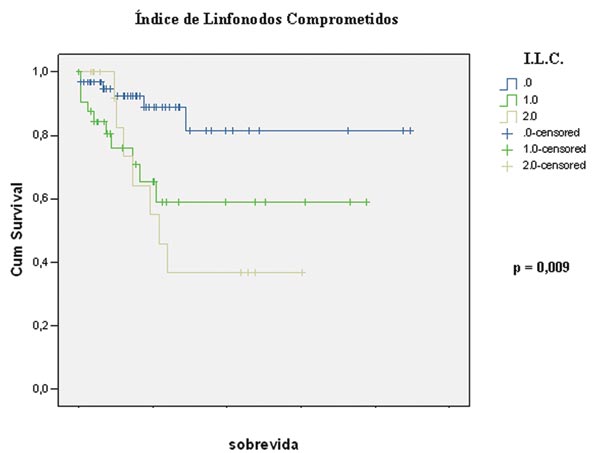 |
Figura 2 - Sobrevida considerando o índice de linfonodos
comprometidos (ILC-0, ILC-1 e ILC-2). |
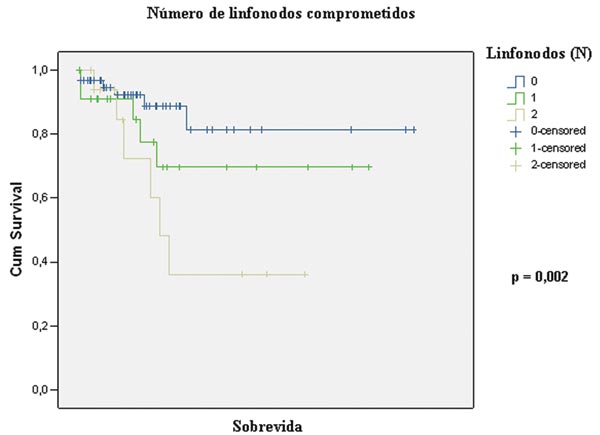 |
Figura 3 - Sobrevida segundo o número de linfonodos
comprometidos (N0, N1, N2). |
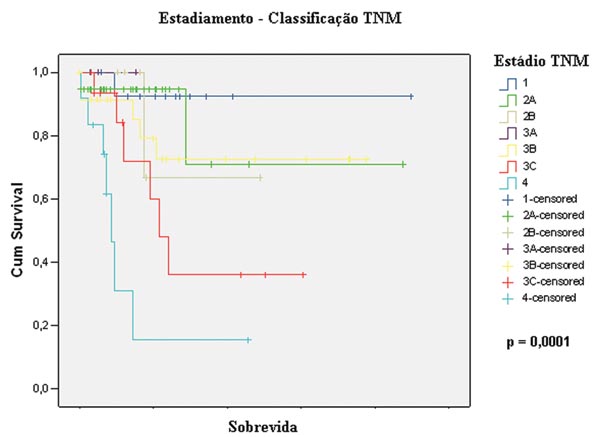 |
Figura 4 - Sobrevida segundo estádios da classificação TNM. |
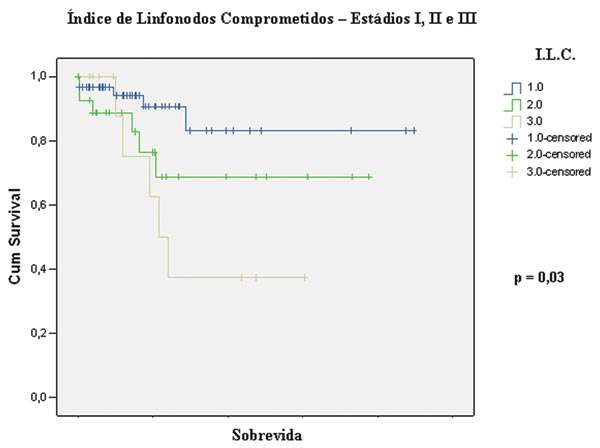 |
Figura 5 - Sobrevida segundo o índice de linfonodos comprometidos nos doentes classificados nos estádios I, II e III da classificação TNM. |
ABSTRACT: In patients with colorectal cancer, the compromising of the lymph node is one of the most important prognostic factors. Aim: The aim of this study is to determine the prognostic independent value of relation between compromised and examined lymph nodes, (LNR) in patients with colorectal cancer. Method: One hundred and thirteen 113 patients (62 women) with colon ad upper rectum cancer were studied. Fifteen patients were staged to the stadium I of the TNM classification, 44 to II, 42 to III and 24 to the stadium IV. The lymph node ratio rate was determined by the relation between total number of compromised and examined lymph nodes. The patients were divided in three groups according to the proportion of compromised lymph nodes: LNR-0: when there was no lymph node involvement; LNR-1: when there was compromising of up to 20% of the examined lymph nodes and LNR-2: when there was compromising in 21% or more of the examined nodes. The relations between lymph node ratio, number of removed lymph nodes and number of compromising lymph nodes by cancer were determined. Patients younger than 18 years old who were submitted to neoadjuvant quimioradiation protocol were excluded as well as the ones who had less than 12 lymph nodes removed. The clinical and histopathological variables were analyzed through descriptive statistic. The correlation between the variables was valued by Spearman correlation test. The five years survival was determined by the tests of Kaplan-Meier, Log-rank and the multivariate analysis of the prognostic variables by the Cox model establishing level of significance of 5 % (p=0.05). Results: There was significant difference in the five years overall survival in patients classified in the different groups of LNR (p=0.009). Patients of the group LNR-0 presented five years overall survival bigger than 80%, while in those classified to the groups LNR-1 and LNR-2, the five years overall survival was less than 60% and 40%, respectively. The number of compromising lymph nodes alone was correlated to the five years overall survival (p=0.03). The multivariate analysis demonstrated that the LNR is an independent prognosis variable of the five years overall survival (p=0.009). There was relation between the total number of compromised lymph nodes and the LNR (p=0.00001, with rs=0.977). Conclusion: The results of the present study showed that the LNR can be considered an independent prognostic variable of overall survival in patients with colorectal cancer.
Key Words: Lymph Nodes, Lymph Node Excision, Prognosis, Colorectal Neoplasms, Survival Analysis, Survival Rate.
Referências
1. Surveillance epidemiology and end results (SEER).
National Cancer Institute. [cited 2008 mar 21]. Avaliable from:
http://seer.cancer.gov/statfacts/html/colorect/html
2. Sanfelippo PM, Beahrs OH. Factors in the prognosis
of adenocarcinoma of the colon and rectum. Arch Surg.1972;104:401-6.
3. Cain AS, Longino LA. Carcinoma of the colon in children.
J Pediatr Surg.1970; 5:527-32.
4. Wolmark N, Wieand HS, Rockette HE, Fischer B, Glass
A, Lawrence W, et al. The prognostic significance of
tumor location and bowel obstruction in Dukes B and C
colorectal cancer. Findings from the NSABP clinical
trials.1983;198:743-52.
5. Grinnel RS. The grading and prognosis of carcinoma of
the colon and rectum. Ann Surg.1939;109:500-33.
6. Dukes CE. The classification of cancer of the rectum.
J Pathol.1932;35:323-32.
7. Astler VB, Coller FA. The prognostic significance of
direct extension of carcinoma of the colon and rectum.
Ann Surg.1954;139:846-51.
8. Dukes CE, Bussey HJR. The spread of rectal cancer and
its effect on prognosis. Br J Cancer.1958;12:309-20.
9. Halvorsen TB, Sein E. Influence of mucinous components
on survival in colorectal adenocarcinomas: a multivariate
analysis. J Clin Pathol.1988;41:1068-72.
10. Martinez CAR, Priolli DG, Cardinalli IA, Piovesam H,
Pereira JA, Waisberg J, et al. Correlação entre o padrão de
distribuição tecidual e os valores séricos do antígeno
carcinoembrionário em doentes com câncer. Rev bras Coloproct.2006; 26:41-53.
11. Cutait R. Contribuição ao estudo do antígeno
carcinoembrionário e dos antígenos de superfície ABH no câncer colo-retal.
Tese (Livre Docência) _ Faculdade de Medicina da Universidade
de São Paulo, São Paulo, 1991. 96p.
12. Khankhanian N, Mavligit GM, Russell WO, Schimek
M. Prognostic significance of vascular invasion in colorectal
cancer of Dukes' B class. Cancer.1977;39:1195-200.
13. Cruz JV, Cutait R, Martinez CAR, Bevilacqua RG, Leite
KRM, Margarido NF. Importância prognostica da invasão neural
no câncer colorretal. Estudo imunoistoquímico com a proteína
S-100. Rev bras Coloproct.2006;26:280-93.
14. Wang Y, Jatkoe T, Zhang Y, Mutch MG, Talantov D, Jiang
J, et al. Gene expression profiles and molecular markers to
predict recurrence of Dukes' B colon cancer. J
Clin Oncol.2004;221:564-71.
15. Sigurdson ER: Lymph node dissection: Is it diagnostic
or therapeutic? J Clin Oncol 2003;21:965-7.
16. Gajra A, Newman N, Gamble GP, Kohman LJ, Graziano SL.
Effect of number of lymph nodes sampled on outcome
in patients with stage I non-small-cell lung cancer. J
Clin Oncol.2003; 21:1029-34.
17. Wong JH, Severino R, Honnebier MB. Number of
nodes examined and staging accuracy in colorectal carcinoma. J
Clin Oncol.1999;17:2896-900.
18. LeVoyer TE, Sigurdson ER, Hanlon AR, Mayer
RJ, MacDonald JS, Catalano PJ. Colon cancer survival
is associated with increasing number of lymph nodes
analyzed: a secondary survey of intergroup trial INT-0089. J
Clin Oncol.2003; 21:2912-9.
19. Celen O, Yildirim E, Berberoglu U. Prognostic impact
of positive lymph node ratio in gastric carcinoma. J
Surg Oncol.2007;96:95-101.
20. Persiani R, Rausei S, Biondi A, Boccia S, Cananzi F, D'Ugo
D. Ratio of metastatic lymph nodes: Impact on staging
and survival of gastric cancer. Eur J Surg Oncol.2007;34:519-24.
21. Herr HW, Bochner BH, Dalbagni G, Donat SM, Reuter
VE, Bajorin DF. Impact of the number of lymph nodes
retrieved on outcome in patients with muscle invasive bladder cancer.
J Urol. 2002;167:1295-8.
22. Weir L, Speers C, D'yachkova Y, Olivotto IA.
Prognostic significance of the number of axillary lymph nodes removed
in patients with node negative breast cancer. J
Clin Oncol.2002;20:1793-9.
23. Berger AC, Watson JC, Ross EA, Hoffman JP. The
metastatic/examined lymph node ratio is an important prognostic
factor after pancreaticoduodenectomy for pancreatic
adenocarcinoma. Am Surg.2004;70:235-40.
24. Lee HY, Choi HJ, Park KJ, Shin JS, Kwon HC, Roh MS,
et al. Prognostic significance of metastatic lymph node ratio
in node-positive colon carcinoma. Ann Surg
Oncol.2007; 14:1712-7.
25. Berger AC, Sigurdson ER, Le Voyer T, Hanlon A, Mayer
RJ, Macdonald JS, et al. Colon cancer survival is associated
with decreasing ratio of metastatic to examined lymph nodes.
J Clin Oncol.2005;23:8706-12.
26. Wang J, Hasset JM, Dayton MT, Kulaylat MN.
Lymphy node ratio: role in the staging of node-positive colon
cancer. Ann Surg Oncol. 2008;15:1600-8.
27. Derwinger K, Carlsson G, Gustavsson B. A study of
lymph node ratio as a prognostic marker in colon cancer. Eur J
Surg Oncol. 2007;34:771-5.
28. Trufelli DC, da Costa Miranda V, Palos CC, Ramos E,
Abrão MN, da Silva VA, et al. Positive /total dissected lymph
nodes ratio as a prognostic factor in colorectal cancer. Rev Ass
Med Bras.2007;53:539-42.
29. Schumacher P, Dineen S, Barnett C Jr, Fleming J, Anthony
T. The metastatic lymph node ratio predicts survival in
colorectal cancer. Am J Surg.2007;194:827-31.
30. Nelson H, Petrelli N, Carlin A, Couture J, Fleshman J,
Guillem J, et al. National Cancer Institute Expert Panel.
Guideline 2000 for Colon and Rectal Cancer Surgery. J Nat
Cancer Inst.2001;93:583-96.
31. SPSS® Inc.; Ilinois, USA
32. Collaborative staging and coding manual. American
Joint Committee on Cancer. [cited 2008 mar 21]. Avaliable in
URL from: http://www.cancerstaging.org
33. Pinho MSL. Estadiamento molecular do câncer colorretal:
o futuro se aproxima. Rev bras Coloproct.2005;25:279-84.
34. Hermanek P, Giedl J, Dworak O. Two programs for
examination of regional lymph nodes in colorectal carcinoma with regard
to the new pN classification. Path Res Pract.1989;185:867-73.
35. Goldstein NS, Sanford W, Coffey M, Layfield LJ.
Lymph node recovery from colorectal resection specimens
removed for adenocarcinoma: Trends over time and a
recommendation for a minimum number of lymph nodes to be recovered. Am
J Clin Pathol.1996;106:209-16.
36. Chen SL, Bilchik AJ. More extensive nodal dissection
improves survival for stages I to III of colon cancer: a
population-based study. Ann Surg.2006;244:602-10.
37. Herrera-Ornelas L, Justiniano J, Castillo N, Petrelli NJ,
Stulc JP, Mittelman A. Metastases in small nodes from colon
cancer. Arch Surg.1987;122:1253-6.
38. Mönig SP, Baldus SE, Zirbes TK, Schröder W,
Lindemann DG, Dienes HP, et al. Lymph node size and
metastatic infiltration in colon cancer. Ann Surg Oncol.1999;6:579-81.
39. Wood TF, Saha S, Morton DL, Tsioulias GJ, Rangel
D, Hutchinson W Jr, et al. Validation of lymphatic mapping
in colorectal cancer: In vivo, ex vivo, and laparoscopic
techniques. Ann Surg Oncol.2001;8:150-7.
40. Wong SL, Ji H, Hollenbeck BR, Morris AM, Baser O,
Birkmeyer JD. Hospital lymph node examination rates and survival
after resection for colon cancer. JAMA.2007;298:2149-54.
41. Schrag D, Panageas KS, Riedel E, Hsieh L, Bach PB,
Guillem JB, et al. Surgeon volume compared to hospital volume as
a predictor of outcome following primary colon cancer
resection. J Surg Oncol.2003;83:68-78.
42. Meyerhardt JA, Castelano PJ, Schrag D, Ayanian JZ,
Haller DG, Mayer RJ, et al. Association of hospital procedure
volume and outcomes in patients with colon cancer at high risk
for recurrence. Ann Inter Med. 2003;139:649-57.
43. Haboubi NY, Clark P, Kaftan SM, Schofield PF.
The importance of combining xylene clearance and immunohistochemistry in the accurate staging of
colorectal carcinoma. J R Soc Med.1992;85:386-8
44. Palma RT, Waisberg J, Bromberg S, Simão AB, Godoy
AC. Micrometastasis in regional lymph nodes of
extirpated colorectal carcinoma: immunohistochemical study
using anti-cytokeratin antibodies AE1/AE3.
Colorectal Dis.2003;5:164-8.
45. Messerini L, Cianchi F, Cortesini C, Comin CE. Incidence
and prognostic significance of occult tumor cells in lymph
nodes from patients with stage IIA colorectal carcinoma. Hum
Pathol. 2006;37:1259-67.
46. Feinstein AR, Sosin DM, Wells CK: The Will
Rogers phenomenon: Stage migration and new diagnostic
techniques as a source of misleading statistics for survival in cancer.
N Engl J Med.1985;312:1604-8.
47. Inoue K, Nakane Y, Iiyama H, Sato M, Kambara T, Nakai
K, et al. The superiority of ratio-based lymph node staging
in gastric carcinoma. Ann Surg Oncol.2002;9:27-34.
48. Bando E, Yonemura Y, Taniguchi K, Fushida S, Fujimura
T, Nishimura G, et al. Outcome of ratio of lymph node
metastasis in gastric carcinoma. Ann Surg Oncol.2002;9:775-84
49. Mammen JM, James LE, Molloy M, Williams A, Wray
CJ, Sussman JJ. The relationship of lymph node dissection
and colon cancer survival in the Veterans Affairs Central
Cancer Registry. Am J Surg.2007:194;349-54.
50. Bui L, Rempel E, Reeson D, Simunovic M. Lymph
node counts, rates of positive lymph nodes, and patient
survival for colon cancer surgery in Ontario, Canada: a
population-based study. J. Surg Oncol.2006;93:439-45.
Endereço para correspondência:
Denise Gonçalves Priolli
Rua São Vicente, 614
Atibaia _ São Paulo _ CEP: 12947-390
Tel/Fax. (11) 4412-7730
e-mail: depriolli@terra.com.br
Recebido em 12/09/2008
Aceito para publicação em 28/09/2008
Trabalho realizado pelo Programa de Pós-Graduação em Ciências da Saúde da Universidade São Francisco, Bragança Paulista, São
Paulo, São Paulo, Brasil.
Trabalho contemplado com o PRÊMIO AB durante o 57º Congresso Brasileiro de Coloproctologia realizado em Gramado (RS) em setembro
de 2008.